13.16. Viết phương trình nhiệt hoá học ứng với sơ đồ biểu diễn biến thiên enthalpy của hai phản ứng...
Câu hỏi:
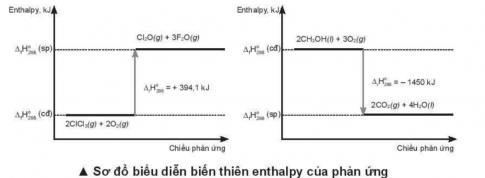
13.16. Viết phương trình nhiệt hoá học ứng với sơ đồ biểu diễn biến thiên enthalpy của hai phản ứng sau:
Câu trả lời:
Người trả lời: GV. Đỗ Đăng Giang
Để giải câu hỏi trên, chúng ta sẽ sử dụng định lý hóa học số lượng như sau:Đưa ra phương trình hóa học của từng phản ứng- Phản ứng 1: 2ClF2 (g) + 2O2 (g) → Cl2O (g) + 3F2O (g)- Phản ứng 2: 2CH3OH (l) + 3O2 (g) → 2CO2 (g) + 4H2O (l)Tính toán enthalpy của từng phản ứng- $\Delta _{r}H_{298}^{o1}$ = +394,10 kJ- $\Delta _{r}H_{298}^{o2}$ = -1450 kJKết hợp phương trình hóa học và enthalpy, chúng ta có:$\Delta _{r}H_{298}^{o_{tong}}$ = $\Delta _{r}H_{298}^{o1}$ + $\Delta _{r}H_{298}^{o2}$ = +394,10 kJ - 1450 kJ = -1055,9 kJVậy phương trình nhiệt hoá học ứng với sơ đồ trên là:2ClF2 (g) + 2O2 (g) + 2CH3OH (l) + 3O2 (g) → Cl2O (g) + 3F2O (g) + 2CO2 (g) + 4H2O (l) $\Delta _{r}H_{298}^{o_{tong}}$ = -1055,9 kJ.
Câu hỏi liên quan:
- 13.1. Cho phương trình nhiệt hoá học của phản ứng.2H2(g) + O2 (g) → 2H2O (l)$\Delta...
- 13.2. Cho phương trình nhiệt hoá học của phản ứng:N2 (g) + O2 (g) → 2NO (g)$\Delta...
- 13.3. Dựa vào phương trình nhiệt hoá học của phản ứng sau:CO2 (g) → CO (g) +...
- 13.4. Phương trình nhiệt hoá học:3H2 (g) + N2 (g) → 2NH3(g) $\Delta _{r}H_{298}^{o}$= - 91,80...
- 13.5. Điều kiện nào sau đây không phải là điều kiện chuẩn?A. Áp suất 1 bar và nhiệt độ 25°C hay 298...
- 13.6. Dựa vào phương trình nhiệt hoá học của các phản ứng sau:CS2 (l) + 3O2 (g) + CO2 (g) + 2SO₂...
- 13.7. Dựa vào phương trình nhiệt hoá học của phản ứng sau:3Fe (s) + 4H2O (l) → Fe3O4 (s) + 4H2 (g)...
- 13.8. a) Enthalpy tạo thành của hợp chất là gì?b) Biến thiên enthalpy trong các phản ứng hoá học là...
- 13.9. Các quá trình sau đây là toả nhiệt hay thu nhiệt?a) Nước hoá rắn.b) Sự tiêu hoá thức ăn.c)...
- 13.10. Hãy nêu 1 phản ứng toả nhiệt và 1 phản ứng thu nhiệt mà em biết.
- 13.11. Khi đun nóng muối ammonium nitrate bị nhiệt phân theo phương...
- 13.12. Một phản ứng mà giá trị của $\Delta _{r}H_{298}^{o}$ > 0 thì phản ứng đó không xảy ra ở...
- 13.13. Cho các đơn chất sau đây: C (graphite, s), Br2 (l), Br2(g), Na (s), Na (g), Hg (l), Hg (s)....
- 13.14. Cho 2 sơ đồ biểu diễn sự thay đổi nhiệt độ theo thời gian của phản ứng (1) và (2). Sơ đồ nào...
- 13.15. Dựa vào Bảng 13.1, sách giáo khoa (SGK) trang 84, viết phương trình nhiệt hoá học của 2 phản...
- 13.17. Cho phản ứng:2ZnS (s) + 3O2 (g) $\overset{t^{o}}{\rightarrow}$ 2CO2 (g) + 4H2O (l) $\Delta...
- 13.18*. Điều chế NH3 từ N2 (g) và H2 (g) làm nguồn chất tải nhiệt, nguồn để điều chế nitric acid và...
- 13.19. Viết phương trình nhiệt hoá học của các quá trình tạo thành những chất dưới đây từ đơn...
- 13.20. Dựa vào Bảng 13.1, sách giáo khoa (SGK) trang 84, sắp xếp các oxide sau đây: Fe2O3 (s),...
Bình luận (0)





