SBT CHƯƠNG 1: CẤU TẠO CỦA NGUYÊN TỬ
SBT CHƯƠNG 2: BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC VÀ ĐỊNH LUẬT TUẦN HOÀN
- Giải bài tập sách bài tập (SBT) bài 5: Cấu tạo của bảng tuần hoàn các nguyên tố hóa học
- Giải bài tập sách bài tập (SBT) bài 6: Xu hướng biến đổi một số tính chất của nguyên tử các nguyên tố trong một chu kì và trong một nhóm
- Giải bài tập sách bài tập (SBT) bài 7: Xu hướng biến đổi thành phần và một số tính chất của hợp chất trong một chu kì
- Giải bài tập sách bài tập (SBT) bài 8: Định luật tuần hoàn. Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học
- Giải bài tập sách bài tập (SBT) bài 9: Ôn tập chương 2
SBT CHƯƠNG 3: LIÊN KẾT HÓA HỌC
- Giải bài tập sách bài tập (SBT) bài 10 Quy tắc Octet
- Giải bài tập sách bài tập (SBT) bài 11 Liên kết ion
- Giải bài tập sách bài tập (SBT) bài 12 Liên kết cộng hóa trị
- Giải bài tập sách bài tập (SBT) Hoá 10 kết nối tri thức bài 13: Liên kết Hydrogen và tương tác Van Der Waals
- Giải bài tập sách bài tập (SBT) Hoá 10 kết nối tri thức bài 14: Ôn tập chương 3
SBT CHƯƠNG 4: PHẢN ỨNG HÓA HỌC
SBT CHƯƠNG 5: NĂNG LƯỢNG HÓA HỌC
SBT CHƯƠNG 6: TỐC ĐỘ PHẢN ỨNG
Giải bài tập sách bài tập (SBT) bài 10 Quy tắc Octet
https://s.shopee.vn/AKN2JyAJAw
Hướng dẫn giải bài 10 Quy tắc Octet trong sách bài tập Hoá học lớp 10
Trong bài 10 Quy tắc Octet trang 28 sách bài tập (SBT) Hoá học 10, chúng ta sẽ tìm hiểu về nguyên tắc quan trọng trong hóa học liên quan đến cấu trúc electron của nguyên tử và phân tử. Bằng cách hướng dẫn chi tiết và giải thích rõ ràng, bài học này sẽ giúp học sinh hiểu rõ hơn về quy tắc Octet và áp dụng chúng vào việc giải các bài tập.
Sách "Kết nối tri thức với cuộc sống" đã được biên soạn theo chương trình đổi mới của Bộ giáo dục, nhằm giúp học sinh tiếp cận kiến thức một cách sinh động và dễ hiểu. Hy vọng rằng với sự hướng dẫn cụ thể và giải thích chi tiết, bài học về Quy tắc Octet sẽ trở nên thú vị và dễ tiếp thu hơn đối với học sinh.
Với việc nắm vững bài học này, học sinh sẽ có thêm kiến thức vững chắc về cấu trúc electron và cân bằng electron trong các phản ứng hóa học. Mong rằng thông qua sách bài tập này, học sinh sẽ phát triển khả năng giải quyết vấn đề và áp dụng kiến thức vào thực tế một cách hiệu quả.
Bài tập và hướng dẫn giải
NHẬN BIẾT
10.1. Liên kết hoá học là
A. sự kết hợp của các hạt cơ bản hình thành nguyên tử bền vững.
B. sự kết hợp giữa các nguyên tử tạo thành phân tử hay tỉnh thể bền vững hơn.
C. sự kết hợp của các phân tử hình thành các chất bền vững.
D. sự kết hợp của chát tạo thành vật thể bền vững.
10.2. Theo quy tắc octet, khi hình thành liên kết hoa học, các nguyên tử có xu hướng nhường, nhận hoặc góp chung electron để đạt tới cấu hình electron bền vững giống như
A. kim loại kiềm gần kề.
B. kim loại kiêm thổ gân kề.
C. nguyên tử halogen gần kề.
D. nguyên tử khí hiếm gần kề.
10.3. Khi hình thành liên kết hoá học, nguyên tử có số hiệu nào sau đây có xu hướng nhường 2 electron để đạt cấu hình electron bền vững theo quy tắc octet?
A.(Z = 12). B.(Z = 9). C.(Z = 11). D.(Z = 10).
10.4. Công thức cầu tạo nào sau đây không đủ electron theo quy tắc octet?
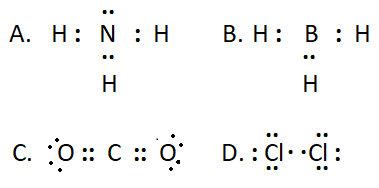
THÔNG HIỂU
10.5. Trong công thức CS2, tổng số cặp electron lớp ngoài cùng của C và S chưa tham gia liên kết là
A.2. B.3. C. 4. D.5.
10.6. Phân tử nào sau đây có các nguyên tử đều đã đạt cấu hình electron bão hoà theo quy tắc octet?
A. BeH2. B. AICl3. C. PCl5. D. SiF4.
10.7. Quy tắc octet không đúng với trường hợp phân tử chất nào sau đây?
A. H2O. B. NO2. C. CO2. D.CI2.
10.8. Trong tự nhiên, các khí hiếm tồn tại dưới dạng nguyên tử tự do. Các nguyên tử của khí hiếm không liên kết với nhau tạo thành phân tử và rất khó liên kết với các nguyên tử của các nguyên tô khác. Ngược lại nguyên tử các nguyên tố khác lại liên kết với nhau tạo thành phân tử hay tinh thể. Giải thích.
10.9. Cấu hình electron lớp ngoài cùng của nguyên tử potassium (kali) là $4s^{1}$,cấu hình electron lớp ngoài cũng của nguyên tử bromine là $4s^{2}4p^{5}$. Làm thế nào các nguyên tử potassinum vá bromine có được cấu hình electron của nguyên tử khi hiếm theo quy tắc octet.
10.10. Khi hình thành liên kết H + CI → HCI và khi phá vỡ liên kết HCI → H + CI thì hệ thu năng lượng hay toả năng lượng. Năng lượng phân tử HCI lớn hơn hay nhỏ hơn năng lượng hệ hai nguyên tử H và CI riêng rẽ? Trong hai hệ đó thì hệ nào bền hơn?
10.11. Trong phân tử Na2S, cấu hình electron của các nguyên tử có tuân theo quy tắc octet không?
VẬN DỤNG
10.12. Vận dụng quy tắc octet để giải thích sự hình thành liên kết trong các phân tử O2, CO2, CaCl2, KBr.
10.13. Đá vôi (thành phần chính là CaCO3) được dùng để sản xuất vôi, trong lĩnh vực xây dựng.... Bariun nitrate Ba(NO3)2 có trong thành phần của kính quang học, gốm, men,.. Phèn đơn aluminium sulfate (thành phần chính là Al2(SO4)3 được sử dụng rộng rãi trong xử lí nước thải, trong công nghệ sản xuất giấy, công nghệ nhuộm vải và công nghệ lọc nước và nuôi trồng thuỷ sản....Dựa vào quy tắc octet, đề xuất công thức cấu tạo của các chất trên.
10.14. Hợp chất X tạo bởi hai nguyên tố A, D có khối lượng phân tử là 76. X là dung môi không phân cực, thường được sử dụng làm nguyên liệu trong tổng hợp chất hữu cơ chứa lưu huỳnh và được sử dụng rộng rãi trong sản xuất vải viscoza mềm. A có công thức hydride dạng AH4 và D có công thức oxide ứng với hoá trị cao nhất dạng DO3.
a) Hãy thiết lập công thức phân tử của X. Biết rằng A có số oxi hoá cao nhất trong X.
b) Đề xuất công thức cấu tạo của X và cho biết các nguyên tử thành phần của X khi liên kết có đủ electron theo quy tắc octet không.
Giải bài tập sách giáo khoa (SGK) 10 Kết nối tri thức
- Soạn văn lớp 10 tập 1 kết nối tri thức
- Soạn văn lớp 10 tập 2 kết nối tri thức
- Văn mẫu lớp 10 kết nối tri thức
- Giải bài tập toán lớp 10 tập 1 kết nối tri thức
- Giải bài tập toán lớp 10 tập 2 kết nối tri thức
- Giải bài tập vật lí lớp 10 kết nối tri thức
- Giải bài tập hóa học lớp 10 kết nối tri thức
- Giải bài tập sinh học lớp 10 kết nối tri thức
- Giải bài tập Địa lí lớp 10 kết nối tri thức
- Giải bài tập lịch sử lớp 10 kết nối tri thức
- Giải bài tập tin học lớp 10 kết nối tri thức
- Giải bài tập Âm nhạc lớp 10 kết nối tri thức
- Giải bài tập mĩ thuật lớp 10 kết nối tri thức
- Giải bài tập giáo dục kinh tế pháp luật lớp 10 kết nối tri thức
- Giải bài tập giáo dục quốc phòng an ninh lớp 10 kết nối tri thức
- Giải bài tập hoạt động trải nghiệm lớp 10 kết nối tri thức
- Giải bài tập thiết kế công nghệ lớp 10 kết nối tri thức
- Giải bài tập công nghệ trồng trọt lớp 10 kết nối tri thức
- Giải bài tập giáo dục thể chất lớp 10 kết nối tri thức
- Giải bài tập tiếng anh lớp 10 Global Success
Giải bài tập sách giáo khoa (SGK) 10 Chân trời sáng tạo
- Soạn văn lớp 10 tập 1 chân trời sáng tạo
- Soạn văn lớp 10 tập 2 chân trời sáng tạo
- Văn mẫu lớp 10 chân trời sáng tạo
- Giải bài tập toán lớp 10 tập 1 chân trời sáng tạo
- Giải bài tập toán lớp 10 tập 2 chân trời sáng tạo
- Giải bài tập vật lí lớp 10 chân trời sáng tạo
- Giải bài tập hóa học lớp 10 chân trời sáng tạo
- Giải bài tập sinh học lớp 10 chân trời sáng tạo
- Giải bài tập Địa lí lớp 10 chân trời sáng tạo
- Giải bài tập lịch sử lớp 10 chân trời sáng tạo
- Giải bài tập tin học lớp 10 chân trời sáng tạo
- Giải bài tập Âm nhạc lớp 10 chân trời sáng tạo
- Giải bài tập mĩ thuật lớp 10 chân trời sáng tạo
- Giải bài tập giáo dục kinh tế pháp luật lớp 10 chân trời sáng tạo
- Giải bài tập Hoạt động trải nghiệm, hướng nghiệp lớp 10 chân trời sáng tạo bản 1
- Giải bài tập Hoạt động trải nghiệm, hướng nghiệp lớp 10 chân trời sáng tạo bản 2
- Giải bài tập giáo dục quốc phòng an ninh lớp 10 chân trời sáng tạo
- Giải bài tập thiết kế công nghệ lớp 10 chân trời sáng tạo
- Giải bài tập công nghệ trồng trọt lớp 10 chân trời sáng tạo
- Giải bài tập giáo dục thể chất lớp 10 chân trời sáng tạo
- Giải bài tập tiếng anh lớp 10 Friends Global
Giải bài tập sách giáo khoa (SGK) 10 Cánh diều
- Soạn văn lớp 10 tập 1 cánh diều
- Soạn văn lớp 10 tập 2 cánh diều
- Văn mẫu lớp 10 cánh diều
- Giải bài tập toán lớp 10 tập 1 cánh diều
- Giải bài tập toán lớp 10 tập 2 cánh diều
- Giải bài tập vật lí lớp 10 cánh diều
- Giải bài tập hóa học lớp 10 cánh diều
- Giải bài tập sinh học lớp 10 cánh diều
- Giải bài tập Địa lí lớp 10 cánh diều
- Giải bài tập lịch sử lớp 10 cánh diều
- Giải bài tập tin học lớp 10 cánh diều
- Giải bài tập Âm nhạc lớp 10 cánh diều
- Giải bài tập mĩ thuật lớp 10 cánh diều
- Giải bài tập giáo dục kinh tế pháp luật lớp 10 cánh diều
- Giải bài tập giáo dục quốc phòng an ninh lớp 10 cánh diều
- Giải bài tập hoạt động trải nghiệm lớp 10 cánh diều
- Giải bài tập thiết kế công nghệ lớp 10 cánh diều
- Giải bài tập công nghệ trồng trọt lớp 10 cánh diều
- Giải bài tập giáo dục thể chất lớp 10 cánh diều
- Giải bài tập tiếng anh lớp 10 Explore new worlds
Giải bài tập sách bài tập (SBT) lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 10 tập 1 kết nối tri thức
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 10 tập 2 kết nối tri thức
- Giải bài tập sách bài tập (SBT) toán lớp 10 tập 1 kết nối tri thức
- Giải bài tập sách bài tập (SBT) toán lớp 10 tập 2 kết nối tri thức
- Giải bài tập sách bài tập (SBT) hóa học lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) sinh học lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) vật lí lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) lịch sử lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) địa lí lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) tin học lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) giáo dục kinh tế pháp luật lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) giáo dục quốc phòng và an ninh lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) hoạt động trải nghiệm lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) tiếng anh lớp 10 Global success
Giải bài tập sách bài tập (SBT) lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 10 tập 1 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 10 tập 2 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) toán lớp 10 tập 1 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) toán lớp 10 tập 2 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) hóa học lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) sinh học lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) vật lí lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) lịch sử lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) địa lí lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) giáo dục kinh tế pháp luật lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) giáo dục quốc phòng và an ninh lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) hoạt động trải nghiệm lớp 10 chân trời sáng tạo bản 1
- Giải bài tập sách bài tập (SBT) hoạt động trải nghiệm lớp 10 chân trời sáng tạo bản 2
- Giải bài tập sách bài tập (SBT) tiếng anh lớp 10 Friends Global
Giải bài tập sách bài tập (SBT) lớp 10 Cánh diều
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 10 tập 1 cánh diều
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 10 tập 2 cánh diều
- Giải bài tập sách bài tập (SBT) toán lớp 10 tập 1 cánh diều
- Giải bài tập sách bài tập (SBT) toán lớp 10 tập 2 cánh diều
- Giải bài tập sách bài tập (SBT) hóa học lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) sinh học lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) vật lí lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) lịch sử lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) địa lí lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) tin học lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) giáo dục kinh tế pháp luật lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) hoạt động trải nghiệm lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) giáo dục quốc phòng và an ninh lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) tiếng anh lớp 10 Explore new world
Giải bài tập chuyên đề học tập 10 Kết nối tri thức
- Giải bài tập chuyên đề toán lớp 10 kết nối tri thức
- Giải bài tập chuyên đề ngữ văn lớp 10 kết nối tri thức
- Giải bài tập chuyên đề vật lí lớp 10 kết nối tri thức
- Giải bài tập chuyên đề hóa học lớp 10 kết nối tri thức
- Giải bài tập chuyên đề sinh học lớp 10 kết nối tri thức
- Giải bài tập chuyên đề lịch sử lớp 10 kết nối tri thức
- Giải bài tập chuyên đề địa lí lớp 10 kết nối tri thức
- Giải bài tập chuyên đề công nghệ trồng trọt lớp 10 kết nối tri thức
- Giải bài tập chuyên đề giáo dục kinh tế và pháp luật lớp 10 kết nối tri thức
- Giải bài tập chuyên đề tin học lớp 10 theo định hướng tin học ứng dụng kết nối tri thức
- Giải bài tập chuyên đề tin học lớp 10 theo định hướng khoa học máy tính kết nối tri thức
- Giải bài tập chuyên đề mĩ thuật lớp 10 kết nối tri thức
Giải bài tập chuyên đề học tập 10 Chân trời sáng tạo
- Giải bài tập chuyên đề toán lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề ngữ văn lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề vật lí lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề hóa học lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề sinh học lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề địa lí lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề lịch sử lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề giáo dục kinh tế và pháp luật lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề âm nhạc lớp 10 chân trời sáng tạo
Giải bài tập chuyên đề học tập 10 Cánh diều
- Giải bài tập chuyên đề toán lớp 10 cánh diều
- Giải bài tập chuyên đề ngữ văn lớp 10 cánh diều
- Giải bài tập chuyên đề vật lí lớp 10 cánh diều
- Giải bài tập chuyên đề hóa học lớp 10 cánh diều
- Giải bài tập chuyên đề sinh học lớp 10 cánh diều
- Giải bài tập chuyên đề địa lí lớp 10 cánh diều
- Giải bài tập chuyên đề lịch sử lớp 10 cánh diều
- Giải bài tập chuyên đề công nghệ trồng trọt lớp 10 cánh diều
- Giải bài tập chuyên đề giáo dục kinh tế và pháp luật lớp 10 cánh diều
- Giải bài tập chuyên đề tin học lớp 10 theo định hướng tin học ứng dụng cánh diều
- Giải bài tập chuyên đề tin học lớp 10 theo định hướng khoa học máy tính cánh diều
- Giải bài tập chuyên đề âm nhạc lớp 10 cánh diều





