Bài tậpCâu 1:Trong các cách biểu diễn electron vào các orbital của phần lớp 2p ở trạng thái...
Câu hỏi:
Bài tập
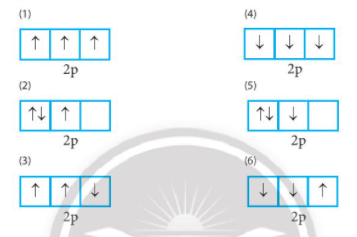
Câu 1: Trong các cách biểu diễn electron vào các orbital của phần lớp 2p ở trạng thái cơ bản, hãy chọn cách phân bố đúng
Câu trả lời:
Người trả lời: GV. Đỗ Đăng Huy
Cách phân bố electron vào các orbital của phần lớp 2p ở trạng thái cơ bản được thực hiện theo nguyên tắc bổ sung electron vào orbital trống trước khi ghép electron vào cùng một orbital.Câu trả lời cho câu hỏi trên:1. Theo nguyên tắc Hund: electron sẽ được phân bố vào các orbital có năng lượng như nhau trước khi ghép vào cùng một orbital. Do đó, trong phần lớp 2p ở trạng thái cơ bản, 3 electron sẽ được phân bố vào 3 orbital 2px, 2py, 2pz một cách độc lập, mỗi orbital chứa 1 electron có cùng spin trước khi bắt đầu ghép electron.
Câu hỏi liên quan:
- Câu hỏi bổ sungHệ Mặt Trời hôm Mặt Trời ở trung tâm và các thiên thể quay quanh theo những quỹ đạo...
- Câu 2:Quan sát Hình 4.3, phân biết khái niệm đám mây electron và khái niệm orbital nguyên tử
- Câu 3:Cho biết khái niệm orbital nguyên tử xuất phát từ mô hình nguyên tử của Rutherford -...
- Câu 4. Quan sát Hình 4.4, hãy cho biết điểm giống và khác nhau giữa các orbital p (px, py, pz)
- II. Lớp và phân lớp electronCâu 5:Quan sát hình 4.5, nhận xét cách gọi tên các lớp electron...
- Câu 6:Từ hình 4.5, cho biết lực hút của hạt nhân với electron ở lớp nào là lớn nhất và lớp...
- Câu 7:Quan sát Hình 4.6, nhận xét về số lượng phân lớp trong các lớp từ 1 đến 4
- III. Cấu hình electron nguyên tửCâu 8:Quan sát Hình 4.7, nhận xét chiều tăng năng lượng của...
- Câu 9:Quan sát Hình 4.8, cho biết cách biểu diễn 2 electron trong một orbital dựa trên cơ sở...
- Câu 10:Quan sát Hình 4.9, hãy cho biết nguyên tử oxygen có bao nhiêu electron ghép đôi vào...
- Câu 11:Từ Bảng 4.1, hãy chỉ ra mối quan hệ giữa số thứ tự lớp và số electron tối đa trong mỗi...
- Câu hỏi bổ sung 1 :Nguyên tử nitrogen có 2 lớp electron trong đó có 2 phân lớp s và 1 phân...
- Câu 12:Quan sát Hình 4.10, hãy nhận xét số lượng electron độc thân ở mỗi trường hợp
- Câu 13:Hãy đề nghị cách phân bố electron vào các orbial để số electron độc thân là tối đa
- Câu hỏi bổ sung 2Trong các trường hợp (a) và (b) dưới đây, trường hợp nào có sự phân bố electron...
- Câu 14:Cấu hình electron của một nguyên tử cho biết những thông tin gì?
- Câu hỏi bổ sung 3Viết cấu hình electron nguyên tử của nguyên tố aluminium (Z = 13) và biểu diễn cấu...
- Câu 15:Quan sát Bảng 4.2, hãy cho biết dựa trên cơ sở nào để dự đoán phosphorus là nguyên tố...
- Câu hỏi bổ sung 3Lithium là một nguyên tố có nhiều công dụng, được sử dụng trong chế tạo máy...
- Câu 2:Cho nguyên tố X có 2 lớp eletron, lớp thứ 2 có 6 electron. Xác định số hiệu nguyên tử...
- Câu 3:Ở trạng thái cơ bản, nguyên tủ của những nguyên tố nào dưới đây có electron độc thân?a)...
- Câu 4:Viết cấu hình electron nguyên tử của các nguyên tố: carbon ( Z=6), sodium (Z=11) và...






Khi đã điền electron cho tất cả các orbital đơn độc, sẽ bắt đầu ghép cặp electron vào các orbital 2p, theo cách phân bố nguyên tố hóa học.
Do đó, cách phân bố đúng của electron vào các orbital 2p là mỗi orbital chứa một electron trước khi bắt đầu ghép cặp electron.
Theo nguyên lý Hund, electron sẽ điền vào orbital đơn độc trước khi điền vào orbital chung với một electron khác.
Trong phần lớp 2p, có 3 orbital là 2px, 2py và 2pz.