21.25. Trong phòng thí nghiệm, khí chlorine được điều chế, làm khô và thu vào bình theo sơ đồ dưới...
Câu hỏi:
21.25. Trong phòng thí nghiệm, khí chlorine được điều chế, làm khô và thu vào bình theo sơ đồ dưới đây.
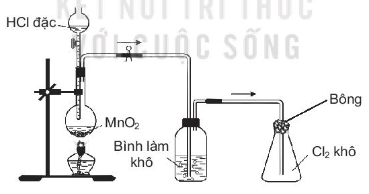
Hãy đề xuất một dung dịch để sử dụng cho từng mục đích sau
a) Cho vào bình làm khô để làm khô khí Cl2.
b) Tẩm vào bông đậy bình thu khí để hạn chế khí Cl2 bay ra.
Giải thích và viết phương trình hoá học minh hoạ nếu có.
Câu trả lời:
Người trả lời: GV. Đỗ Hồng Long
Cách làm:
1. Xác định yêu cầu của bài toán: cần chọn dung dịch phù hợp để làm khô khí Cl2 và để hạn chế khí Cl2 bay ra.
2. Xem xét các yếu tố cần lưu ý: dung dịch cần không tác dụng với Cl2 và cần có tính chất phản ứng phù hợp với mục đích sử dụng của nó.
3. Đề xuất chọn dung dịch H2SO4 đặc để làm khô khí Cl2 vì H2SO4 có khả năng hút nước mạnh mẽ và không tác dụng với Cl2.
4. Đề xuất chọn dung dịch NaOH 4% để hạn chế khí Cl2 bay ra vì NaOH có tính kiềm và có thể tác dụng với Cl2 để tạo ra sản phẩm NaCl và NaClO.
Câu trả lời cho câu hỏi:
a) Để làm khô khí Cl2, chúng ta chọn dung dịch H2SO4 đặc.
b) Để hạn chế khí Cl2 bay ra, chúng ta chọn dung dịch NaOH 4%.
Phương trình hoá học minh hoạ:
2NaOH + Cl2 → NaCl + NaClO + H2O.
1. Xác định yêu cầu của bài toán: cần chọn dung dịch phù hợp để làm khô khí Cl2 và để hạn chế khí Cl2 bay ra.
2. Xem xét các yếu tố cần lưu ý: dung dịch cần không tác dụng với Cl2 và cần có tính chất phản ứng phù hợp với mục đích sử dụng của nó.
3. Đề xuất chọn dung dịch H2SO4 đặc để làm khô khí Cl2 vì H2SO4 có khả năng hút nước mạnh mẽ và không tác dụng với Cl2.
4. Đề xuất chọn dung dịch NaOH 4% để hạn chế khí Cl2 bay ra vì NaOH có tính kiềm và có thể tác dụng với Cl2 để tạo ra sản phẩm NaCl và NaClO.
Câu trả lời cho câu hỏi:
a) Để làm khô khí Cl2, chúng ta chọn dung dịch H2SO4 đặc.
b) Để hạn chế khí Cl2 bay ra, chúng ta chọn dung dịch NaOH 4%.
Phương trình hoá học minh hoạ:
2NaOH + Cl2 → NaCl + NaClO + H2O.
Câu hỏi liên quan:
- NHẬN BIẾT 21.1. Số electron ở lớp ngoài cùng của mỗi nguyên tử nguyên tố halogen làA. 5....
- 21.2. Tính chất hoá học đặc trưng của các đơn chất halogen làA. tính khử. ...
- 21.3. Trong tự nhiên, nguyên tố fluorine tồn tại phổ biến nhất ở dạng hợp chất làA. Na3AlF6...
- 21.4. Ở điều kiện thưởng, halogen tồn tại ở thể rắn, có màu đen tím làA. F2. ...
- 21.5. Muối nào có nhiều nhất trong nước biển với nồng độ khoảng 3%?A. NaCl. ...
- 21.6. Số oxi hoá cao nhất mà nguyên tử chlorine thể hiện được trong các hợp chất làA. -1....
- 21.7. Các nguyên tố halogen thuộc nhóm nào trong bảng tuần hoàn?A. VIIIA. ...
- 21.8. Trong nhóm halogen, đơn chất có tính oxi hoá mạnh nhất làA. F2. ...
- 21.9. Khi đun nóng, chất thăng hoa chuyển từ thể rắn sang thể hơi màu tím làA. F2....
- 21.10. Halogen nào sau đây được dùng để khử trùng nước sinh hoạt ?A. F2. ...
- 21.11. Trong cơ thể người, nguyên tố iodine tập trung ở tuyến nào sau đây?A. Tuyến thượng...
- 21.12. Trong dãy halogen, nguyên tử có độ âm điện nhỏ nhất làA. fluorine. ...
- THÔNG HIỂU21.13. Trong nhóm halogen, từ fluorine đến iodine, bán kính nguyên tử biến đổi như thế...
- 21.14. Trong nhóm halogen, nguyên tửnguyên tố thể hiệnkhuynh hướng nhận1 electron...
- 21.15. Trong nhóm halogen, từ fluorine đến iodine, nhiệt độ nóng chảy biến đổi như thế nào?A. Giảm...
- 21.16. Halogen phản ứng mãnh liệt với hydrogen ngay cả trong bóng tối làA. F2. ...
- 21.17. Khi tác dụng với kim loại, các nguyên tử halogen thể hiện xu hướng nào sau đây?A....
- 21.18. Hít thở không khí có chứa khí nào sau đây vượt ngưỡng 30μg/$m^{3}$ không khí (QCVN ...
- 21.19. Quá trình sản xuất khí chlorine trong công nghiệp hiện nay dựa trên phản ứng nào sau...
- 21.20. Chỉ thị nào sau đây thường dùng để nhận biết dung dịch I2?A. Phenolphtalein. ...
- VẬN DỤNG21.21. Thực nghiệm cho thấy các phản ứng:H2 (g) + X2 (g)→ 2HX (g)trong dãy halogen...
- 21.22. Đốt cháy hoàn toàn 0,48 g kim loại M (hoá trị II) bằng khí chlorine, thu được 1,332 g muối...
- 21.23. Nung nóng một binh bằng thép có chứa 0,04 mol H2 và 0,04 mol Cl2 để thực hiện phản ứng, thu...
- 21.24. Có hai ống nghiệm, mỗi ống chứa 2 mL dung dịch muối X của kali. Cho vài giọt dung dịch AgNO3...
Bình luận (0)





