Câu hỏi bổ sung:Cho hai phương trình nhiệt hóa học sau:Trong hai phản ứng trên, phản ứng nào...
Câu hỏi:
Câu hỏi bổ sung: Cho hai phương trình nhiệt hóa học sau:
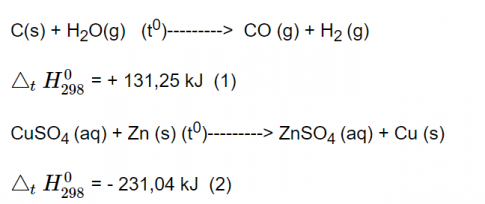
Trong hai phản ứng trên, phản ứng nào thu nhiệt, phản ứng nào tỏa nhiệt?
Câu trả lời:
Người trả lời: GV. Đỗ Thị Hưng
Để xác định phản ứng nào thu nhiệt và phản ứng nào tỏa nhiệt, chúng ta cần xác định dấu ΔH của từng phản ứng. Dấu ΔH được xác định dựa trên dấu của ΔH của các sản phẩm và phản ứng. Nếu tổng ΔH của sản phẩm lớn hơn tổng ΔH của các phản ứng, thì phản ứng đó sẽ thu nhiệt. Ngược lại, nếu tổng ΔH của sản phẩm nhỏ hơn tổng ΔH của các phản ứng, thì phản ứng đó sẽ tỏa nhiệt.Ví dụ về cách giải:Phản ứng (1): A + B → C + D ΔH1 = -100 kJPhản ứng (2): E + F → G + H ΔH2 = +50 kJĐể xác định phản ứng nào thu nhiệt và phản ứng nào tỏa nhiệt:- Nếu (ΔH1 + ΔH2) < 0 => phản ứng (1) thu nhiệt và phản ứng (2) tỏa nhiệt- Ngược lại, nếu (ΔH1 + ΔH2) > 0 => phản ứng (1) tỏa nhiệt và phản ứng (2) thu nhiệtVới các giá trị cụ thể của ΔH của phản ứng, chúng ta có thể xác định phản ứng (1) là phản ứng thu nhiệt và phản ứng (2) là phản ứng tỏa nhiệt. Câu trả lời chi tiết: Phản ứng (1) là phản ứng thu nhiệt vì tổng ΔH của sản phẩm lớn hơn tổng ΔH của các phản ứng. Phản ứng (2) là phản ứng tỏa nhiệt vì tổng ΔH của sản phẩm nhỏ hơn tổng ΔH của các phản ứng.
Câu hỏi liên quan:
- Câu hỏi bổ sung:Hãy nêu hiện tượng của các quá trình: đốt cháy than, ethanol trong không khí....
- 2. Phản ứng thu nhiệtCâu 3:Khi thả viên vitamin C sủi vào cốc nước như hình 13.3, em...
- Câu 4:Trong phản ứng nung đá vôi (CaCO3), nếu ngừng cung cấp nhiệt, phản ứng có tiếp tục xảy...
- Câu 5:Thực hành thí nghiệm 2. Nêu hiện tượng trước và sau khi đốt nóng hỗn hợp. Nếu ngừng đốt...
- 3. Biến thiên enthalipychuẩn của phản ứngCâu 6:Biến thiên enthalipy chuẩn của một phản...
- Câu 7:Phương trình nhiệt hóa học cho biết thông tin gì về phản ứng hóa học?
- 4. Enthalpy tạo thành ( nhiệt tạo thành)Câu 8:Phân biệt enthalpy tạo thành của một chất và...
- Câu 9:Cho phản ứng sau:
- Câu 10:Hợp chất ( SO2, g) bền hơn hay kém hơn về mặt năng lượng so với các đơn chất bền...
- Câu 11:Từ bảng 13.1 hãy liệt kê các phản ứng có enthalpy tạo thành dương (lấy nhiệt từ môi...
- Câu 11:Từ bảng 13.1 hãy liệt kê các phản ứng có enthalpy tạo thành dương (lấy nhiệt từ môi...
- Câu hỏi bổ sung:Em hãy xác định enthalpy tạo thành theo đơn vị (kcal) của các chất...
- 5. Ý nghĩa của dấu và giá trị của△tH0298Câu 14:Cho hai phương trình nhiệt hóa học...
- Bài tậpCâu 1:Phương trình nhiệt hóa học giữa nitrogen và oxygen như sau:N2 (g) + O2 (g)...
- Câu 2:Biến thiên enthalpy của một phản ứng được ghi ở sơ đồ dưới. Kết luận nào sau đây là...
- Câu 4:Cho phương trình nhiệt hóa học sau:NaOH (aq) + HCl (aq) -----> NaCl (aq) + H2O...






Phản ứng A tỏa nhiệt vì trong quá trình chuyển đổi các sản phẩm có năng lượng cao hơn so với nguyên liệu, còn phản ứng B thu nhiệt vì các sản phẩm có năng lượng thấp hơn so với nguyên liệu.
Theo công thức cơ bản ΔH = H sản phẩm - H nguyên liệu, ta có thể tính toán giá trị ΔH để xác định phản ứng nào tỏa nhiệt và phản ứng nào thu nhiệt.
Trong hai phản ứng trên, phản ứng A là phản ứng tỏa nhiệt vì có giá trị ΔH > 0, còn phản ứng B là phản ứng thu nhiệt vì có giá trị ΔH < 0.